據悉,2019年2月28日,Glycom A/S公司根據法規(EU)2015/2283第10(1)條規定向歐盟委員會提交申請書,申請批準3’-唾液乳糖鈉鹽(3’-Sialyllactose)作為新資源食品。該原料是通過轉基因菌株大腸桿菌K12 DH1微生物發酵而來,可用于原味巴氏滅菌牛奶、飲料、谷物棒、嬰配產品、食品補充劑等方面。
2019年6月12日,歐盟委員會要求歐洲食品安全局(EFSA)根據法規(EU)2015/2283第10(3)條對3’-唾液乳糖鈉鹽作為新資源食品進行安全性風險評估。經過對科學試驗和毒理學數據資料分析,歐盟食品安全局官方于2020年3月25日發表該原料作為新資源食品安全性的科學意見。
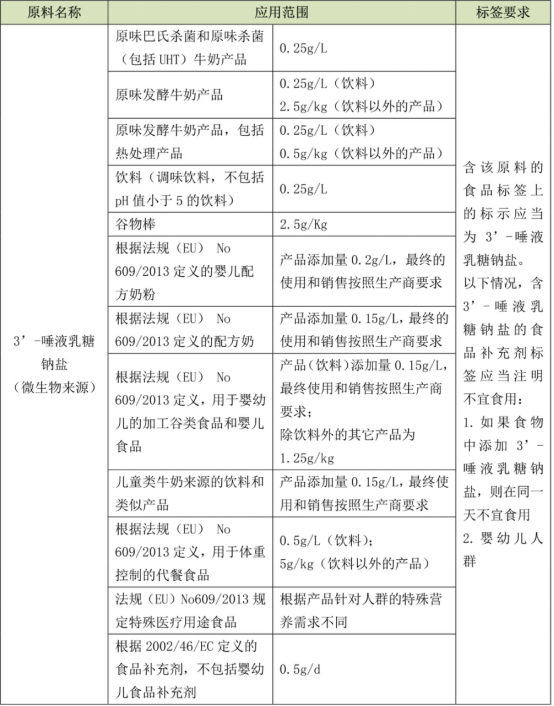
2021年1月28日,歐盟委員會發布法規(EU)2021/96號條例,批準3’-唾液乳糖鈉鹽作為新資源食品,并修訂歐盟委員會實施條例(EU)2017/2470附件涉及新型食品使用要求,詳見下表。
同時,2021年1月25日,歐盟發布條例(EU) 2021/50,批準2'-巖藻糖乳糖和二巖藻糖乳糖混合物(2′-fucosyllactose/difucosyllactose mixture)作為新型食品的擴展用途,本條例自發布之日起第二十天生效。
法規(EU) 2017/2470表格1增加以下條目:

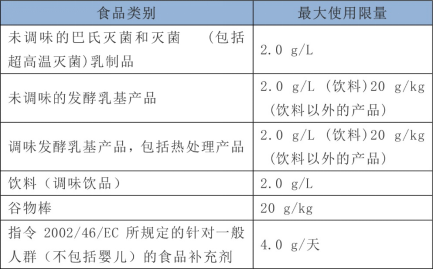
據了解,歐盟于2019年11月29日發布(EU)2019/1979號條例,批準2'-巖藻糖乳糖/二巖藻糖乳糖混合物(2‘‐fucosyllactose/difucosyllactose mixture)作為新型食品投放市場。主要修訂如下: 將2'-巖藻糖乳糖/二巖藻糖乳糖混合物將列入實施法規(EU)2017/2470中建立的授權新型食品的清單中。使用食品類別大使用限量如下表所示。
在線咨詢